Fermentai
apibrėžimas
Fermentai yra cheminės medžiagos, kurių galima rasti visame kūne. Jie organizme išjudina chemines reakcijas.
istorija
Žodis fermentas padarė Vilhelmas Friedrichas Kühne'as 1878 m ir yra kilęs iš graikų pagaminto žodžio enzymon, kuris reiškia mieles arba raugą. Tada jis atsidūrė tarptautiniame moksle. tarptautinė grynosios taikomosios chemijos sąjunga (IUPAC) ir tarptautinė biochemijos sąjunga (IUBMB) kartu sukūrė fermentų nomenklatūrą, kurioje šios didelės medžiagų grupės atstovai apibūdinami kaip bendra grupė. Pavadinimas, kuris klasifikuoja fermentus pagal jų užduotis, yra svarbus nustatant atskirų fermentų užduotis.
Fermentų iliustracija
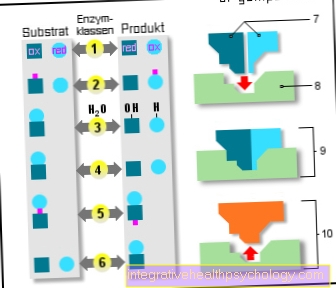
Fermentai
6 fermentų klasės:
- Oksidoreduktazės
(Oksidacija / redukcija) - Transferazės
(Užkrato pernešimas) - Hidrolazės
(Vandens naudojimas) - Liazės
(Skilimas) - Izomerazės
(ta pati empirinė formulė) - Ligazės
(Papildymo reakcijos) - Pagrindai
- Aktyvus centras
- Fermentas / substratas
kompleksas - Fermentas / produktas
kompleksas
Visų apžvalgaDr-Gumperto atvaizdus galite rasti: medicininės iliustracijos
Pavadinimas
Pavadinimas fermentas yra įjungtas trys pagrindiniai principai pagrįstas. Fermentų pavadinimai, besibaigiantys -ase, apibūdina keletą sistemos fermentų. Pats fermento pavadinimas apibūdina fermento sukeltą reakciją (katalizuojamas). Fermento pavadinimas taip pat yra fermento klasifikacija. Be to, kodų sistema, kuri EB numerių sistema, kuriame fermentai gaminami pagal skaitmeninį kodą keturi skaičiai galima rasti. Pirmasis skaičius nurodo fermentų klasę. Visų aptiktų fermentų sąrašai užtikrina, kad nurodytą fermento kodą galima rasti greičiau. Nors kodai yra pagrįsti fermento katalizuojamos reakcijos savybėmis, praktiškai skaitiniai kodai yra nepatogūs. Dažniau vartojami sistemingi pavadinimai, remiantis aukščiau pateiktomis taisyklėmis. Nomenklatūros problemų kyla, pavyzdžiui, su fermentais, kurie katalizuoja kelias reakcijas. Todėl kartais jiems yra keli pavadinimai. Kai kurie fermentai turi nereikšmingus pavadinimus, kurie nerodo, kad paminėta medžiaga yra fermentas. Kadangi pavadinimai tradiciškai buvo plačiai naudojami, kai kurie iš jų išliko.
Klasifikacija pagal fermentų funkciją
Pagal IUPAC ir IUBMB, fermentai yra suskirstyti į šešias fermentų klases pagal jų sukeltą reakciją:
- Oksidoreduktazės
Oksidoreduktazės sukelia redokso reakcijas. Vykdant šią cheminę reakciją, elektronai perduodami iš vieno reakcijos partnerio į kitą. Viena medžiaga išskiria elektronus (oksidacija), kita medžiaga priima elektronus (redukciją).
Katalizuojamos reakcijos formulė yra A ?? + B? A? + B?.
A medžiaga išskiria elektroną (?) Ir oksiduojasi, o medžiaga B sugeria šį elektroną ir yra redukuota. Štai kodėl redokso reakcijos dar vadinamos redukcijos-oksidacijos reakcijomis.
Daugelis medžiagų apykaitos reakcijų yra redoksinės reakcijos. Oksigenazės perduoda vieną ar kelis deguonies atomus į savo substratą. - Transferazės
Transferazės perneša funkcinę grupę iš vieno substrato į kitą. Funkcinės grupės yra atominės organinių junginių grupės, kurios daugiausia lemia medžiagos savybes ir reakcijos elgesį. Cheminiai junginiai, turintys tas pačias funkcines grupes, yra grupuojami į medžiagų klases dėl jų panašių savybių. Funkcinės grupės bus suskirstytos pagal tai, ar jie yra heteroatomai, ar ne. Heteroatomai yra visi organinių junginių atomai, kurie nėra nei anglis, nei vandenilis.
Pvz .: -OH -> hidroksilo grupė (alkoholiai) - Hidrolazės
Hidrolazės skaido jungtis grįžtamosiomis reakcijomis, naudodamos vandenį. Esteriai, esteriai, peptidai, glikozidai, rūgščių anhidridai arba C-C jungtys. Pusiausvyros reakcija yra: A-B + H2O? A-H + B-OH.
Fermentas, priklausantis hidrolazių grupei, yra alfa galaktozidazė. - Liazės
Liazės, dar vadinamos sintazėmis, katalizuoja kompleksinių produktų suskaidymą iš paprastų substratų, neatskiriant ATP. Reakcijos schema yra A-B → A + B.
ATP yra adenozino trifosfatas ir nukleotidas, susidedantis iš adenozino nukleozido trifosfato (ir kaip tokio energijos turinčio nukleorūgšties RNR blokelio). Tačiau ATP daugiausia yra universali bet kurioje ląstelėje esančios energijos forma, kuri tuo pačiu metu yra svarbus energijos tiekimo procesų reguliatorius. Jei reikia, ATP sintezuojamas iš kitų energijos atsargų (kreatino fosfatas, glikogenas, riebalų rūgštys). ATP molekulę sudaro adenino liekana, cukraus ribozė ir trys fosfatai (? To?) Esteryje (?) Arba anhidrido jungtys (? Ir?). - Izomerazės
Izomerazės pagreitina izomerų cheminę konversiją. Izomerija yra dviejų ar daugiau cheminių junginių, turinčių visiškai tuos pačius atomus (ta pati empirinė formulė) ir molekulinės masės, atsiradimas, tačiau jie skiriasi atomų jungtimi ar erdviniu išdėstymu. Atitinkami junginiai vadinami izomerais.
Šie izomerai skiriasi savo cheminėmis ir (arba) fizikinėmis savybėmis, taip pat dažnai ir biocheminėmis savybėmis. Izomerija pirmiausia pasireiškia organiniais junginiais, bet ir su (neorganiniais) koordinaciniais junginiais. Izomerija skirstoma į skirtingas sritis. - Ligazės
Ligazės katalizuoja cheminių medžiagų susidarymą, kurie yra chemiškai sudėtingesni už naudojamus substratus, tačiau, priešingai nei liazės, fermentiniu požiūriu veiksmingi tik skaidant ATP. Šių medžiagų susidarymui reikalinga energija, kuri gaunama skaidant ATP.
Kai kurie fermentai sugeba katalizuoti kelias, kartais labai skirtingas reakcijas. Tokiu atveju jie priskiriami kelioms fermentų klasėms.
Jus taip pat gali sudominti šie straipsniai:
- Alfa-gliukozidazė
- Lipazė
- Tripsinas
Klasifikacija pagal fermentų struktūrą
Beveik visi fermentai yra baltymai ir juos galima klasifikuoti pagal baltymų grandinės ilgį:
- Monomerai
Fermentai, kurie susideda tik iš vienos baltymo grandinės - Oligomerai
Fermentai, susidedantys iš kelių baltymų grandinių (monomerai) - Daugelio fermentų grandinės
Keli agreguoti fermentai, kurie bendradarbiauja ir reguliuoja vienas kitą. Šios fermentų grandinės katalizuoja vėlesnius ląstelės metabolizmo etapus.
Be to, yra atskirų baltymų grandinių, turinčių keletą fermentų aktyvumų; jie vadinami daugiafunkciais fermentais.
Klasifikacija pagal kofaktorius
Kita klasifikacija yra klasifikacija pagal kofaktorių įvertinimą. Kofaktoriai, kofermentai ir substratai yra įvairių medžiagų klasifikatorių pavadinimai, kurie, sąveikaudami su fermentais, daro įtaką biocheminėms reakcijoms.
Aptariamos organinės molekulės ir jonai (daugiausia metalo jonai).
Grynus baltymų fermentus sudaro tik baltymai, o aktyvusis centras susidaro tik iš aminorūgščių liekanų ir peptido pagrindo. Aminorūgštys yra organinių junginių klasė, turinti bent vieną karboksi grupę (-COOH) ir vieną amino grupę (-NH2).
Holoenzimai susideda iš baltymo komponento - apoenzimo ir kofaktoriaus - mažos molekulinės masės molekulės (ne baltymo). Abi kartu yra svarbios fermento funkcijai.
Kofermentai
Organinės molekulės kaip kofaktoriai vadinamos kofermentais. Jei jie yra kovalentiškai susieti su apoenzimu, jie vadinami protezavimo grupėmis arba bendrais substratais. Protezinė grupė reiškia ne baltymų komponentus, tvirtai (dažniausiai kovalentiškai) sujungtus su baltymu, turinčiu katalizinį poveikį.
Kosubstratai yra įvairių medžiagų klasifikatorių pavadinimai, kurie, sąveikaudami su fermentais, daro įtaką biocheminėms reakcijoms. Kaip biokatalizatoriai, molekulės pagreitina organizmų reakcijas, fermentai - biochemines reakcijas. Jie sumažina aktyvacijos energiją, kurią reikia įveikti, kad medžiaga galėtų virsti.